- Структуры, для описания объемных данных
- Сегментация
- Рендеринг поверхностей
- Рендеринг на основе вокселей
- Рендеринг на основе преобразований
В различных областях медицины все более широкое распространение получают сегодня методы визуализации внутренних структур человека на основе данных томографических исследований. Эти методы компьютерной графики называются визуализацией объема. В статье приводится обзор методов, используемых для каждого из этапов конвейера визуализации объема, при этом особое внимание уделяется структурам данных, методам сегментации и методам рендеринга, в основе которых лежит либо представление поверхности объекта, либо его воксельное представление. Методы иллюстрируются примерами из различных областей медицины: черепно - лицевой хирургии, травматологии, нейрохирургии, радиотерапии и медицинском образовании.
На протяжении двух последних десятилетий технология медицинской интроскопии (medical imaging) или технология получения изображений внутренних органов человека пережила ряд принципиальных изменений. Ранее в распоряжении врачей были лишь рентгеновские снимки, которые давали некоторое представление об исследуемых органах в виде наложения теней на изображениях. Эти изображения отличались плохой контрастностью и отсутствием какой-либо информации о глубине объектов. Использование компьютеров дало возможность развиваться новым направлениям томографической интроскопии, таким как компьютерная томография (CT-computed tomography), магнитная резонансная томография (MRI-magnetic resonance imaging) и позитронная эмиссионная томография (PET-positron emission tomography). С помощью томографической аппаратуры можно получить снимки множества сечений тела пациента, которые характеризуют особенности его анатомии и физиологии. Эти снимки с чрезвычайной четкостью показывают различные органы, причем изображения органов не налагаются друг на друга. Математические методы позволяют реконструировать трехмерную структуру органов по множеству параллельных сечений.
Во многих случаях для установления диагноза врач зрительно анализирует изображения отдельных сечений объекта, полученных при томографическом обследовании. Однако, для некоторых клинических задач, подобных хирургическому планированию, необходимо понимать 3D структуру во всей ее сложности и видеть дефекты. Опыт показал, что "умозрительная реконструкция" объектов по изображениям их сечений чрезвычайно трудна и сильно зависит от опыта и воображения наблюдателя. В таких случаях хотелось бы представить человеческое тело так, как его увидел бы хирург или анатом.
Цель использования метода визуализации объема в медицине - создание точных и реалистичных визуальных представлений объектов по медицинским данным. Получаемые в результате изображения, даже если они по-существу двухмерные, часто называют 3D изображениями или 3D реконструкциями для того, чтобы отличать их от 2D сечений или обычных рентгеновских снимков. Аналогичные подходы применяются также для экспериментальных и модельных данных, которые получают в других областях, таких как динамика жидкостей, геология и метеорология [1].
Методы визуализации
Приведем обзор методов, используемых при визуализации объема. На рис. 1. показаны все фазы конвейера визуализации объема. После получения серии томографических изображений частей тела пациента данные обычно подвергаются некоторым процедурам предобработки для преобразования и, возможно, фильтрации. Дальнейшая обработка может следовать несколькими путями.
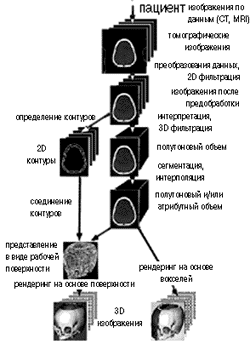
Рисунок 1.
Этапы конвейра визуализации объема. При использовнаии конкретных методов
отдельные шаги обработки могут быть опущены, совмещены или переставлены
местами.
Пунктирной линией на рис. 1. представлены ранние подходы, в которых объект реконструировался по контурам на изображениях сечений. В остальных методах, обозначенных толстой линией, процесс построения изображений начинается непосредственно с объемных данных, заданных на регулярной сетке. При необходимости, путем интерполяции можно обеспечить одинаковый шаг выборки данных по всем трем измерениям. Для улучшения качества объем можно подвергнуть процедуре фильтрации, подобно тому, как это делается при обработке 2D изображений.
Следующий шаг состоит в идентификации различных объектов, представленных в объемных данных так, чтобы их можно было выделить для визуализации или, наоборот, сделать невидимыми. Этот шаг включает сегментацию и интерпретацию. Простейший способ состоит в бинаризации данных с использованием порога интенсивности, например, для выделения костей из других тканей в компьютерной томографии. Однако, в некоторых случаях, особенно при использовании данных MRI, требуются более изощренные методы сегментации.
После сегментации существует выбор, какой из методов рендеринга использовать далее. Более традиционные подходы, которые основаны на представлении объектов их поверхностями, сначала создают промежуточную модель, выделяя поверхности объекта. Далее выполняется рендеринг с использованием любого стандартного метода машинной графики. Относительно недавно были разработаны подходы, основанные на воксельном представлении объемов, которые создают трехмерные изображения объекта непосредственно из объемных данных. Эти методы используют полную информацию о значениях интенсивности полутонового изображения для рендеринга поверхностей, разрезов или прозрачных и полу-прозрачных объемов. Оба эти подхода имеют свои достоинства. Решение о том, какой из методов следует использовать для конкретного приложения, зависит как от размера памяти и мощности компьютера, так и от целей визуализации. Недавно был разработан новый подход к визуализации объема, использующий методы рендеринга, основанные на преобразованиях.
Структуры, для описания объемных данных
Наиболее важными структурами для описания объемных данных являются:
Сегментация
Полутоновой объем обычно включает большое число различных структур, затеняющих друг друга. Для того, чтобы изобразить одну из них, следует решить, какую часть данных необходимо использовать, а какую игнорировать. В идеале, выбор должен быть сделан с помощью команды типа "покажи только мозг". Однако, для этого требуется, чтобы компьютер знал, какие части объема (или, точнее, какие воксели) относятся к мозгу, а какие нет.
Первым шагом распознавания объекта должно быть разделение полутонового объема на разные области, которые являются однородными по отношению к некоторому формальному критерию и соответствуют реальным (анатомическим) объектам. Такой процесс называется сегментацией. Для представления результатов подходящей структурой данных является обобщенная воксельная модель. На следующем шаге интерпретации, области могут быть идентифицированы и соотнесены осмысленным понятиям, таким как "белое вещество" или "желудочек".
Все методы сегментации можно разделить на два типа: "бинарные" и "нечеткие", в соответствии с тем, какая логика положена в основу: бинарная или нечеткая. При бинарной сегментации ответ на вопрос, принадлежит ли воксель определенной области, всегда да или нет. Такая информация является предпосылкой, например, для создания поверхностного представления по объемным данным. Однако, недостатком метода является то, что он не справляется со случаями неопределенности или случаями, когда объект занимает только часть вокселя. В случае нечеткой сегментации не обязательно принимать точное решение "да" или "нет" - каждому вокселю приписываются вероятности того, что он принадлежит той или иной материи.
Сейчас имеется большое количество методов сегментации для 3D медицинских изображений, которые можно разбить на три типа: методы на основе точек, границ и областей. При сегментации на основе точек, воксели классифицируются только в соответствии с величиной их интенсивности. Хорошо известны такие методы, как распознавание паттернов [3] и нейронные сети [4]. При сегментации на основе границ, в изображаемом объеме определяют неоднородности в распределении интенсивности, используя для этого первые или вторые производные. При сегментации на основе областей, рассматриваются свойства целых областей, такие как размер или форма. Часто используется комбинация нескольких разных подходов.
Хотя, безусловно, конечной целью является автоматическая сегментация, методы, существующие сегодня, все еще недостаточно надежны, чтобы должным образом работать в любых ситуациях. Поэтому на практике часто более полезны удобные интерактивные системы (рис. 2).

Рисунок 2.
3D изображение плода по данным MRI. С использованием
системы интерактивной сегментации было определено около 50 объектов.
Рендеринг поверхностей
Ключевой идеей этого вида рендеринга является построение промежуточного описания поверхности требуемых объектов по объемным данным, используя для этого результаты сегментации. Если в качестве элементов поверхности используются треугольники, то этот процесс называется триангуляцией. Построенное описание используется затем для рендеринга.
К явным достоинствам методов на основе поверхностей можно отнести очень большое уменьшение количества данных при переходе от объемного представления к поверхностному. Время рендеринга также может быть уменьшено, если при формировании поверхности используются общепринятые структуры данных, такие как сетки с треугольными ячейками, рендеринг которых поддерживается программными и аппаратными средствами. С другой стороны, на этапе реконструкции поверхности отбрасывается большое количество ценной информации, содержащейся в изображениях сечений. Если представление в виде поверхности уже сформировано, вернуться назад и получить исходные значения интенсивности невозможно. Разрезы объекта в этом представлении бессмысленны, так как информации о его внутренней части нет. Кроме того, каждое изменение критериев для определения поверхности, например, порогов, требует пересчета всей структуры данных.
Реконструкция поверхности из объема. Первый метод, который широко использовался в клинической практике, был разработан в конце 70-х [5]. Полутоновой объем сначала бинаризуется с использованием порога интенсивности. Затем создается список граней вокселей, расположенных на границе между вокселями, принадлежащими внутренней и наружной частям объекта. Можно показать, что результирующие поверхности всегда хорошо определены и замкнуты. Описание поверхности, сформированное по данному алгоритму совсем простое - все грани имеют одинаковый размер и форму, и могут быть ориентированы только шестью различными способами. Конечно, такой метод дает только грубое приближение к настоящей форме объекта. Поэтому на результирующем 3D изображении отсутствуют многие тонкие детали.
Позже были предложены методы, которые используют всю полутоновую информацию. В алгоритме марширующих кубов, разработанном Лоренсеном и Клайном, рассматривается куб объемных данных, состоящий из 222 смежных вокселей [6]. В зависимости от того, один или больше таких вокселей содержится внутри объекта (их значения выше пороговой величины), строится часть поверхности, состоящая из не более, чем четырех треугольников, и помещается внутрь куба. Точная локализация треугольников находится путем линейной интерполяции интенсивностей в вершинах вокселей. В результате получается поверхность с большим количеством деталей и разрешением выше воксельного (рис.3). Ориентация поверхности вычисляется по градиенту интенсивности.
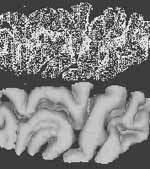
Рисунок 3.
3D изображение части мозга, полученное с использованием алгоритма марширующих
кубов, техники триангуляции (вверху) и закраски (внизу) по данным MRI.
При применении алгоритма марширующих кубов к клиническим данным создаются сотни тысяч треугольников. Было показано, что число этих треугольников может быть значительно уменьшено путем последующего упрощения треугольной сетки без большой потери информации.
Закраска. В общем плане, закраска - это получение реалистического изображения объекта исходя из положения, ориентации и характеристик его поверхностей и с учетом освещающих его источников света. Отражающие свойства поверхности описываются с помощью модели освещенности, например, модели Фонга, которая учитывает свойства рассеянного, диффузного и зеркального света. Наиболее существенными входными данными таких моделей является локальная ориентация поверхности, задаваемая векторами нормалей. Способ вычисления нормали к поверхности в методе марширующих кубов и описывается ниже. Альтернативный способ - использовать нормали треугольников, составляющих поверхность.
Рендеринг на основе вокселей
При рендеринге на основе вокселей изображение формируется непосредственно из объемных данных. Основное преимущество этого метода по сравнению с методами на основе поверхностей, заключается в том, что вся начальная информация об интенсивностях сохраняется в течение процесса рендеринга. Это делает данный метод идеальной техникой для интерактивного исследования данных. При этом интерактивно можно менять величины порогов и другие параметры, которые изначально не известны. Кроме того, рендеринг на основе вокселей позволяет комбинировать изображения разных типов: непрозрачные и полупрозрачные поверхности, разрезы и проекции максимальных интенсивностей. Недостатком методов на основе вокселей является необходимость обрабатывать большое количество данных. Это не позволяет решать прикладные задачи на современных компьютерах в реальном времени. Однако, с применением специальных аппаратных средств уже сейчас можно достичь скоростей несколько кадров в секунду.
Сканирование объема. Способы воксельного рендеринга различаются, главным образом, стратегией сканирования: пиксель за пикселем (упорядочение по изображению) или воксель за вокселем (упорядочение по объему). При сканировании с упорядочиванием по изображению объемные данные выбираются на лучах вдоль направления наблюдения. Этот метод известен как метод отслеживания луча:
FOR каждого пикселя на плоскости изображения DO
FOR каждой точки на луче зрения DO
Вычислить вклад в пиксель
Основные положения данного метода иллюстрируются на рис. 4. Вдоль луча легко определяется видимость поверхностей и объектов. Луч может остановиться, когда на его пути встречается непрозрачная поверхность.

Рисунок 4.
Метод отслеживания луча для визуализации объема. В этом случае для
нахожденияповерхности объекта используется порог интенсивности.
Метод отслеживания луча является очень гибким и хорошо понятным приемом сканирования. Сравнительно легко совмещать методы рендеринга для непрозрачных, полупрозрачных и прозрачных поверхностей. Кроме того, сканирование по изображению можно одновременно использовать для рендеринга как воксельных, так и поверхностных данных. Качество изображения можно изменять, увеличивая или уменьшая шаг выборки данных. Все иллюстрации, представленные в данной статье получены с использованием алгоритма отслеживания луча.
С другой стороны, применимость алгоритмов отслеживания луча ограничивается требованиями большого объема памяти и высокой мощности компьютера. Для того, чтобы объект можно было рассматривать с различных направлений, необходимо обеспечить произвольный доступ ко всем входным объемным данным. Кроме того, для косых лучей требуется интерполяция интенсивностей в точках выборки данных. Для уменьшения времени вычислений процедуру рендеринга начинают с малой плотности выборки данных, чтобы быстро сгенерировать результирующий вид. Если пользователь не вносит каких-либо изменений, то плотность выборки данных постепенно увеличивается до максимального разрешения. Другой прием использует то, что большое количество времени тратится на трассировку пустого пространства вдали от изображаемых объектов. Если ограничивать лучи так, чтобы сканировать данные только внутри предопределенного объема вокруг рассматриваемых объектов, то время сканирования сильно уменьшается.
При сканировании с упорядочиванием по объему входные объемные данные выбираются вдоль строк и столбцов 3D массива и производится проецирование выбранного вида на плоскость изображения в направлении наблюдения.
FOR каждой точки объема DO
FOR каждого пикселя ее проекции DO
Вычислить вклад в пиксель
Объем можно сканировать, начиная с вокселей, находящихся на максимальном расстоянии от плоскости изображения и кончая вокселями с минимальным расстоянием (back-to-front - BTF), либо в обратном порядке (front-to-back - FTB). В обоих случаях несколько вокселей могут проецироваться в один и тот же пиксель. Если необходимо изобразить непрозрачную поверхность, следует определить, какие части будут видимыми. При использовании техники BTF, значения пикселей просто замещаются новыми, так что появляются только видимые поверхности. При технике FTB пиксели, которые уже были записаны, сохраняются с помощью z-буфера.
Сканируя данные в том же порядке, в котором они и хранятся, эти методы являются достаточно быстрыми даже для компьютеров с небольшой оперативной памятью. Они особенно подходят для параллельной обработки. До сих пор большей гибкостью при комбинировании разных способов изображений обладали алгоритмы отслеживания луча. Однако, уже разработаны новые методы рендеринга объема, использующие упорядочивание по объему.
Закраска поверхностей. Применяя один из описанных методов сканирования, можно определить видимую поверхность объекта, используя, например, порог. Известен алгоритм закраски, который очень точно вычисляет вектора нормали к поверхности. Из-за эффекта частичного заполнения объема, интенсивность вокселей, лежащих на поверхности, определяется вкладом разных материалов, находящихся внутри вокселей. Градиент результирующей интенсивности может быть, таким образом, использован для вычисления склонения поверхности. Во всех иллюстрациях, приведенных в данной статье, для закраски использовался этот метод.
Плоскости разрезов. Если поверхность объекта получена, то очень простым и эффективным методом визуализации его внутренних структур является построение разрезов. Когда исходные величины интенсивности отображаются на плоскость разреза, их легче понять в анатомическом контексте. Особым случаем является избирательный разрез, для которого определенные объекты исключаются (рис. 5).
Рисунок 5.
3D изображение мозга по данным MRI. Исходные величины интенсивностей
отображаются на плоскости разрезов.
Интегральная проекция и проекция максимальных интенсивностей. Другой способ заглянуть внутрь объекта - это проинтегрировать величины интенсивностей вдоль направления луча зрения. Если при этом использованы все объемные данные, то такой способ - шаг назад к старой технике рентгенограмм. Однако, если такая проекция строится лишь по выбранным данным, то в некоторых случаях результат оказывается полезным.
Для маленьких ярких объектов, подобных сосудам, зарегистрированных методом магнитно-резонансной ангиографии (MRA), больше подходит метод проекции максимальных интенсивностей (maximum intensity projection (MIP)) (рис. 6). При этом подходе вдоль каждого луча по объемным данным определяются значения максимальной интенсивности, которые затем проецируются на плоскость изображения. Достоинство метода заключается в том, что при его использовании не требуется ни сегментация, ни закраска - процедуры, которые могут плохо работать для мелких сосудов. Однако у такого подхода есть и недостатки: так как MIP совсем не учитывает отражение света, результирующие изображения не дают реалистического трехмерного восприятия объектов. Пространственное восприятие можно улучшить, вращая объект, комбинируя отображения с разных поверхностей или плоскостей разреза.
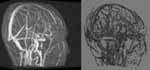
Рисунок 6.
3D изображения сосудов головы по данным магнитной резонансной ангиографии
(MRA). Хотя проекция максимальных интенсивностей (слева) выявляет больше
деталей объекта, пространственное восприятие значительно лучше при использовании
пороговой сегментации и закраски на основе градиента (справа).
Рендеринг объема. В области визуализации рендеринг объема является эквивалентом нечеткой сегментации. Впервые этот подход были использованы для медицинских приложений в 1988 году [7, 8]. Моделью, которая обычно используется для рассмотрения этого подхода, является окрашенный полупрозрачный гель, со взвешенными в нем отражающими частицами. Проходя через объем, лучи освещения частично отражаются и меняют цвет. Для каждого вокселя определяется цвет и непрозрачность. Непрозрачность получается как произведение двух функций: "функции весов объекта" и "функции весов градиента". Функция весов объекта обычно зависит от уровня интенсивности, однако, может быть получена с использованием более изощренного алгоритма нечеткой сегментации. Функция весов градиентов выделяет поверхности для 3D изображений. Все воксели закрашиваются с использованием метода градиента интенсивностей. Значения закраски взвешиваются и суммируются вдоль луча зрения.
Так как при рендеринге объема не производится бинаризация данных, результирующие изображения получаются очень гладкими и с большим количеством тонких деталей (рис. 7). Другим важным достоинством метода является то, что даже для грубо определенных объектов можно осуществить рендеринг с приемлемым качеством. С другой стороны, более или менее прозрачные образы, полученные с помощью методов рендеринга объема, часто тяжело понять, поэтому их клиническое применение может быть ограниченным. Однако, пространственное восприятие можно улучшить путем вращения объекта. Другая проблема возникает из-за большого числа параметров, которые необходимы для определения весовой функции. Кроме того, рендеринг объема - сравнительно медленная процедура: операции взвешивания и закраски проводятся на каждом луче для многих вокселей.
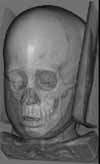
Рисунок 7.
Изображение ребенка с краниосиностозом (trigonocephalon), полученное
по данным СТ методом рендеринга объема. Полупрозрачная визуализация деталей
позволяет увидеть много различных структур, таких как поверхности кожи
и костей, однако пространственное восприятие сильно затруднено.
Рендеринг на основе преобразований
Оба метода рендеринга, как на основе поверхностей, так и на основе вокселей, работают в трехмерном пространстве. Однако, 3D изображения можно получить, исходя и из других представлений данных. Один из таких методов - рендеринг в частотных областях, который создает 3D изображения в пространстве Фурье. Это очень быстрый метод, однако его применимость ограничена достаточно простыми интегральными проекциями.
Более перспективный подход использует вейвлетные преобразования (wavelet tranforms). Эти методы создают мультимасштабное представление 3D объектов, что позволяет локально регулировать размеры отображаемых деталей. Таким образом можно очень сильно сократить количество данных и время рендеринга.
Приложения
На первый взгляд, можно было ожидать, что основной областью для применения методов визуализации объема станет диагностическая рентгенология. Однако, это оказалось не так. Одна из причин заключается в том, что рентгенологи уже обладают большим опытом при анализе двумерных изображений сечений. Другая причина связана с тем, что многие диагностические задачи, такие как определение и классификация опухолей, могут быть достаточно точно решены с помощью томографических изображений. Кроме того, для 3D визуализации объектов по данным MRI необходимы мощные алгоритмы сегментации, которых все еще нет.
По другому обстоят дела в тех областях, в которых терапевтическое решение по рентгенографическим изображениям должен принимать не врач-рентгенолог. Основной областью для применения методов визуализации объема является черепнолицевая хирургия. Визуализация объема не только облегчает понимание патологических условий, но также является полезным инструментом для планирования оптимальных хирургических подходов и косметических результатов вмешательства.
Другой важной областью применения является травматология (рис. 8). В критических случаях время принятия решения должно быть очень малым. С внедрением новых быстрых видов интроскопии и ростом мощности компьютеров, появляется возможность пользоваться методами визуализации объема и в тяжелых случаях. Считается, что визуализация объема особенно полезна в хирургии таза, где морфология усложняет доступ к нужным областям.
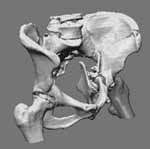
Рисунок 8.
3D изображение таза со множеством переломов по данным СТ с полуфронтальным
направлением луча зрения.
Приложением, которое становится все более привлекательным с увеличением разрешения и специфичности MRI, является нейрохирургическое планирование. В этом случае проблема связана с выбором правильного пути доступа к повреждению. 3D визуализация тканей мозга по данным MRI и кровеносных сосудов по данным MRA до хирургического вмешательства позволяет хирургу найти путь доступа с минимальным риском. Если при этом используется 3D координатный дигитайзер, то собранная с его помощью информация может в какой-то степени направлять действия хирурга в ходе операции. Для облегчения локализации повреждения совмещают использование методов визуализации объема и функциональную информацию, полученную из PET изображений.
Другим потенциальным применением, уменьшающим риск терапевтического вмешательства, является планирование радиотерапии. В этом случае необходимо сфокусировать объектив так, чтобы облучался только необходимый объем, не затрагивая здоровые органы. 3D визуализация объема-мишени, близколежащих органов и моделирование доз радиации позволяют проводить реалистичные репетиции лечебной процедуры.
Приложениями, не связанными непосредственно с клинической работой, являются медицинские исследования и образование. 3D атласы мозга, показанные на рис. 5 и 9, изготовлены по данным MRI и представляются пользователю, как некий интеллектуальный объем. Структурные и функциональные компоненты мозга можно изучать на экране компьютера, подобно тому, как это делается при реальном анатомировании. Сейчас готовятся и другие атласы. Если для их подготовки используются срезы мозга, полученные с помощью криогенной техники (такие срезы были изготовлены в проекте "Видимый Человек" Национальной медицинской библиотеки США), то получается еще более детальная и реалистичная модель (рис. 10).
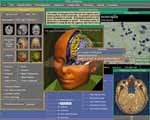
Рисунок 9.
Изучение анатомии путем рассечения медицинских объектов на экране компьютера:
интерфейс пользователя системы VOXEL-MAN/brain. Объем можно произвольно
повернуть и разрезать. Указывая на изображенную поверхность, можно выделить
определенную область и снабдить ее примечаниями. Пользователь может также
по желанию изобразить объекты, выбранные из базы знаний.
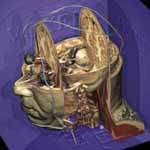
Рисунок 10.
Анатомирование с использованием системы Видимый Человек.
Выводы
Методы визуализации объема в медицине прошли длинный путь развития от первых экспериментов до современных методов рендеринга, позволяющих демонстрировать тонкие детали объектов. По мере совершенствования алгоритмов рендеринга и увеличения точности результирующих картинок, 3D изображения становятся не просто красивыми иллюстрациями, а мощным источником информации для врачей. В некоторых областях медицины, например, таких, как черепнолицевая хирургия или травматология, визуализация объема все больше становится частью стандартных предоперационных процедур. Ожидается дальнейшее быстрое развитие методов визуализации объема.
Ряд проблем все еще мешают более широкому использованию методов визуализации объема в медицине. Во-первых, современные рабочие станции еще не способны создавать 3D изображения достаточно быстро. В течение нескольких лет с ростом мощности компьютеров эта проблема будет решена.
Второй важной проблемой этого подхода является создание такого интерфейса пользователя, который бы устраивал врачей. Сегодня существует большое количество чисто технических параметров, например, для управления сегментацией и закраской. Признание рассмотренного подхода медицинским сообществом наверняка будет зависеть от прогресса в этой области.
Третья проблема связана с методами сегментации объемов в имеющие смысл части, которые представляют различные объекты. На сегодняшний день не существует надежных автоматических методов, которые бы хорошо работали во всех случаях, особенно, для данных MRI. Как было показано, продолжаются исследования в разных направлениях для решения этой задачи.
В ближайшем будущем, при визуализации объема методы рендеринга на основе поверхностей, по-видимому, уступят место более мощным и гибким методам на основе вокселей. Кроме того, могут быть внедрены в практику новые методы визуализации, такие как рендеринг на основе преобразований. Следует ожидать, что станут рабочими и более сложные системы, использующие не только визуализацию, например системы хирургического моделирования и обучающие системы.
Можно представить, что в более отдаленном будущем будет учитываться и функциональная информация (движение, нагрузка и др.), и даже динамически изменяющаяся во времени (4D интроскопия). Другая вызывающая интерес идея состоит в совмещении визуализации объема с современными достижениями в системах виртуальной реальности, которые будут давать возможность врачу ходить или летать вокруг виртуального пациента. Будущее покажет, какой из этих новых подходов окажется действительно полезным для клинической практики.
Литература
[1] Kaufman, A. (Ed.): Volume Visualization. IEEE Computer Society Press, Los Alamitos, CA, 1991.
[2] Laur, D., Hanrahan, P.: Hierarchical splatting: A progressive refinement algorithm for volume rendering. Comput. Graphics 25, 4 (1991), 285-288.
[3] Gerig, G., Martin, J., Kikinis, R., K"ubler, O., Shenton, M., Jolesz, F. A.: Automating segmentation of dual-echo MR head data. In Colchester, A. C. F., Hawkes, D. (Eds.): Information Processing in Medical Imaging, Proc. IPMI "91, Lecture Notes in Computer Science 511, Springer-Verlag, Berlin, 1991, 175-187.
[4] Haring, S., Viergever, M. A., Kok, J. N.: A multiscale approach to image segmentation using Kohonen networks. In Barrett, H. H., Gmitro, A. F. (Eds.): Information Processing in Medical Imaging, Proc. IPMI "93, Lecture Notes in Computer Science 687, Springer-Verlag, Berlin, 199 , 212-224.
[5] Chen, L. S., Herman, G. T., Reynolds, R. A., Udupa, J. K.: Surface sh ding in the cuberille environment. IEEE Comput. Graphics Appl. 5, 12 (1985), 33-43.
[6] Lorensen, W. E., Cline, H. E.: Marching cubes: A high resolution 3D surface construction algorithm. Comput. Graphics 21, 4 (1987), 163-169.
[7] Drebin, R. A.,Carpenter, L., Hanrahan, P.: Volume rendering. Comput. Graphics 22, 4 (1988), 65-74.
[8] Levoy, M.: A hybrid ray tracer for rendering polygon and volume data. IEEE Comput. Graphics Appl. 10, 2 (1990), 33-40